Hvað eru frumefni?
Frumefni samanstanda af atómum sem öll hafa sama fjölda róteinda í atómkjarna sínum. Auk þess er að finna nifteindir og rafeindir í atómum. Fjöldi róteinda og nifteinda ræður eðlismassa þeirra. Frumefnum er raðað niður eftir því hve margar róteindir eru í kjarna þeirra. Þetta er kallað sætistala frumefnanna og ræður stöðu þeirra í lotukerfinu.
Sem dæmi má nefna kolefni sem samanstendur einvörðungu af kolefnisatómum sem hafa sex róteindir í kjarna og þar með sætistöluna 6 í lotukerfinu.
Hvað eru frumeindir?
Árið 1913 setti Niel Bohr fram atómkenningu sína sem lýsti því hvernig atóm samanstendur af kjarna sem inniheldur eina eða fleiri róteindir. Kjarninn inniheldur oft einnig eina eða fleiri nifteindir. Fyrir utan að ráða sætistölunni hefur fjöldi róteinda og nifteinda einnig vægi fyrir eðlismassa frumeindarinnar.
Í kringum kjarnann eru atómhvolf, þar sem rafeindirnar raða sér niður. Á innsta hvolfi geta mest verið tvær rafeindir. Á ysta hvolfinu geta verið alls átta rafeindir á sveimi umhverfis kjarnann.
Þegar ysta hvolfið er fyllt með átta rafeindun er um að ræða afar stöðugt frumefni sem hvarfast ógjarnan við önnur frumefni. Þetta á meðal annars við um eðalgastegundir en ysta rafeindahvolf þeirra er fullt og þar með eru þær afar stöðugar.
Atómkenning Niels Bohs er ennþá gildandi, þó segja megi að ekki sé lengur litið á rafeindirnar sem skipulagðar í hvolfum, heldur fremur sem eins konar iðandi rafeindaský.
Frumefni samanstanda af atómum sem samanstanda af róteindum, nifteindum og rafeindum.
Hvað eru til mörg frumefni?
Alls eru til 118 mismunandi frumefni og af þeim má finna 92 í náttúrunni, meðan afgangurinn er mannanna verk.
Frumefni geta hvarfast saman og þannig tengst – myndað efnatengingu – á ótal mismunandi vegu. Vatn, H2O, er dæmi um efnatengingu þar sem tvær vetnisfrumeindir hafa hvarfast við súrefnisatóm.
Sætistala frumefnanna, efnafræðileigir eiginleikar og geta þeirra til að mynda efnatengingar er sett upp í lotukerfinu.
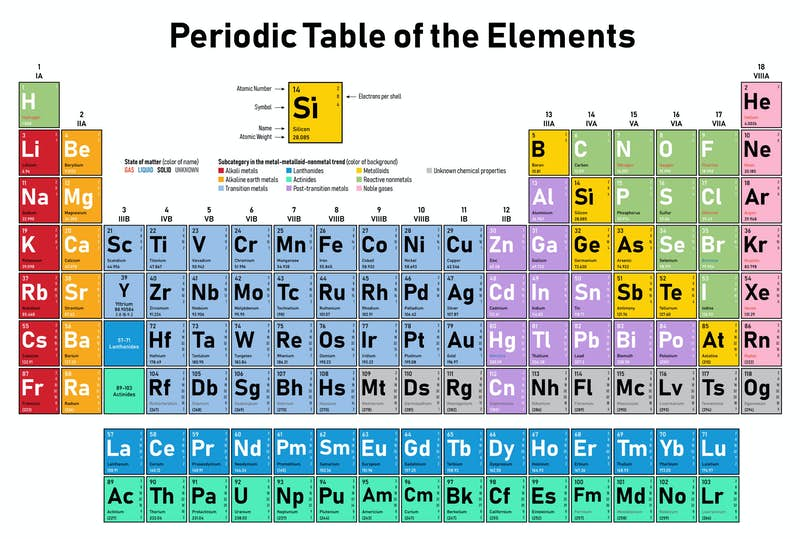
Lotukerfið raðar frumefnunum þannig að auðvelt er að sjá hvernig mismunandi efni hvarfast hvert við annað.
Geislavirk frumefni
Sum frumefni hafa til að bera þann eiginleika að vera geislavirk. Slík frumefni hafa of margar nifteindir í atómkjarnanum miðað við fjölda róteinda. Þetta gerir frumefnin óstöðug og til að endurskapa stöðugleika senda þau frá sér geislun – eða hrörna.
Til eru þrjár gerðir af geislun:
- Alfageislun
- Betageislun
- Gammageislun
Geislavirk efni eru hættuleg, því þau senda frá sér geislun með svo mikilli orku að geislunin getur rifið rafeindir frá atómum og sameindum sem öðlast þá rafhleðslu – svokallaðar jónir. Ef allur líkaminn, einstök líffæri eða frumur verða fyrir geislavirkni geta þau skaddast.
Hvað er samsæta?
Eins og áður hefur komið fram hafa frumeindir sem tilheyra sama frumefni, ævinlega sama fjölda róteinda. Fjöldi nifteinda getur hins vegar verið breytilegur og frumefni með sama fjölda róteinda og frábrugðinn fjölda nifteinda nefnast samsætur.
Samsætur geta ýmist verið þyngri eða léttari en upprunalegt frumefni. Ef nifteindirnar eru færri þá er samsætan léttari en séu nifteindirnar fleiri þá er samsætan þyngri en í upprunalegu frumefni.
Samsætur af sama frumefni hafa sömu efnafræðilegu eiginleikana. Ef það er mikið ójafnvægi milli róteinda miðað við fjölda nifteinda í kjarnanum geta samsæturnar verið geislavirkar og óstöðugar og þannig hrörnað niður í önnur efni. Þetta gagnast mönnum m.a. með geislavirku samsætunni kolefni-14 sem má nota til að aldursgreina ýmsa fornleifafundi.
Léttasta frumefnið, vetni, hefur aðeins þrjár samsætur og er þar með efni sem finnst í fæstum útgáfum. Sesín og xenon hafa 36 samsætur og eru þau efni sem hafa flestar samsætur.
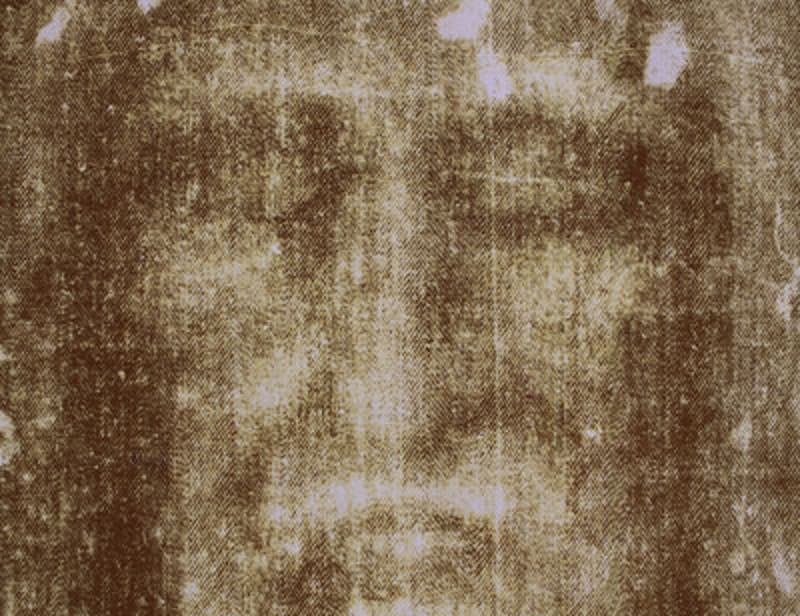
Kolefni-14 aðferðin hefur afhjúpað að líkklæðið frá Tórínó er ekki frá því þegar Jesús dó, heldur frá miðöldum einhvern tíma milli áranna 1260 og 1390.
Hver uppgötvaði fyrst frumefni?
Frumefni eins og gull, silfur, blý og kvikasilfur hafa verið þekkt um aldaraðir og enginn veit hver uppgötvaði þau. Fyrsta örugga sögulega heimildin um uppgötvun frumefnis er frá árinu 1669, þegar þýski alkemistinn – en það voru menn sem leituðust við að búa til gull úr óæðri málmum –Henning Brand, uppgötvaði efnið fosfór í sínu hreina formi.
Í leit sinni að gulli lét hann sneisafulla fötu með eigin þvagi standa í marga daga. Síðan sauð hann vökvann niður í þykka kvoðu og að lokum var gumsið hitað upp í eimingarflösku úr kopar þar til hún var glóandi heit. Gufuna sem steig upp úr henni lét hann þéttast með kælingu.
Hugmynd hans var sú að nú ættu gullmolar að koma í ljós. Þess í stað fann hann hvítleitt vaxkennt efni sem lýsti í myrkri. Hann nefndi efnið fosfór sem á grísku merkir lýsandi.
Þrátt fyrir að ekki hafi verið um gull að ræða eftir allt þetta erfiði auðgaðist hann samt sem áður á uppgötvun sinni. Hann hélt nefnilega uppskriftinni leynilegri og seldi efnið dýrum dómum hinum þýska lækni Johannes Daniel Kraft sem ferðaðist um og sýndi þetta nýstárlega og sjálflýsandi efni aðlinum í Evrópu.
Segja má að nútímaleg efnafræði hafi fyrst komið fram með tilraunum Frakkans Antoine Lavoisiers sem hann gerði upp úr 1770. Með þessum tilraunum varð efnafræði að nákvæmri vísindagrein og á næstu 100 árum uppgötvuðu menn tugi frumefna sem vísindamenn reyndu síðan að skipa niður eftir eiginleikum þeirra.



